- BIOÉNERGÉTIQUE
- BIOÉNERGÉTIQUELa bioénergétique ne diffère pas dans son essence de l’énergétique physique. Il n’y est question que d’échanges et de conversion d’énergie: énergie chimique, travail, chaleur, lumière. Ces échanges, ces transformations, sont soumis au principe de la conservation de l’énergie et au principe de l’accroissement global de l’entropie.La bioénergétique diffère, cependant, de l’énergétique classique ou thermodynamique par diverses modalités. Elle se déroule à température sensiblement constante, avec l’intervention d’une machinerie spéciale: enzymes, transporteurs d’électrons, dont la nature, souvent protéique, d’une part ne tolère pas les fortes élévations thermiques et, d’autre part, possède une activité catalytique puissante à la température ordinaire. Cette activité s’exerce en milieu aqueux et procède par paliers, en effectuant des retouches successives des métabolites, avec souplesse, au niveau des structures compliquées des organites cellulaires.Les sources d’énergiePour leur entretien et leur développement, pour extraire du milieu où ils vivent les aliments dont ils se nourrissent, les êtres vivants ont besoin d’énergie. Selon leurs caractéristiques trophiques, la source d’énergie à laquelle ils puisent est différente. Les végétaux chlorophylliens utilisent la lumière; ils élaborent, par photosynthèse, des composés carbohydrogénés – glucose, amidon – qui possèdent une énergie libre de formation élevée. Leur genèse correspond à la réduction du gaz carbonique par l’eau, selon une réaction globale telle que:
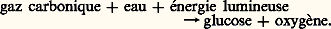 La formation d’une molécule-gramme de glucose correspond à une accumulation d’énergie équivalente à 2 900 kJ, dans l’air, à la pression atmosphérique.Diverses bactéries, autotrophes également, tirent l’énergie qui leur est nécessaire de l’oxydation de substances minérales présentes dans le sol ou les eaux: sels ammoniacaux, nitrates, sulfures... Leur chimiosynthèse est beaucoup moins importante quantitativement que la photosynthèse, aussi la majeure partie de l’énergie externe captée par les êtres vivants provient-elle originellement de la lumière solaire.Les organismes hétérotrophes, animaux, bactéries, champignons, oxydant des substances organiques élaborées par les autotrophes, utilisent l’énergie de liaison chimique des substances synthétisées par les précédents. Les cellules non chlorophylliennes des végétaux autotrophes font de même.Une des caractéristiques des phénomènes bioénergétiques est qu’ils se réalisent à température sensiblement constante. Cela est exact pour nos propres cellules, bien que leur respiration s’accompagne d’une production de chaleur. Mais l’excédent en est immédiatement dissipé.Il en est à peu près de même pour un végétal. Si sa marge thermique interne n’est pas soumise à une régulation aussi poussée que celle de notre corps, cet organisme fonctionne cependant à température sensiblement uniforme dans une gamme comprise entre 0 et 40 0C.Les principes de la thermodynamique et la bioénergétiqueHistoriquement, les phénomènes énergétiques ont d’abord été étudiés à propos des machines à vapeur. Une science s’est ainsi édifiée, qui s’applique à tous les domaines de la physique, de la chimie et de la biologie. Son importance est fondamentale et son application universelle, bien qu’elle ait conservé le nom de thermodynamique.La thermodynamique repose sur deux principes qui ne sont pas directement démontrables avec précision. On considère, cependant, qu’ils sont amplement vérifiés par l’ensemble des conséquences qu’on en a tirées.Le premier principe , ou principe de la conservation de l’énergie , énonce que l’énergie ne peut être ni créée, ni détruite, et que, notamment, la chaleur et le travail en sont deux formes équivalentes. Un système physique (ou un être vivant) qui échange de l’énergie avec l’extérieur subit une variation de son énergie interne. La somme de chaleur perdue et de travail effectué par le système considéré est intégralement reçue par ce qui l’entoure. La validité de ce principe, en biologie, s’impose aisément à l’esprit, même dans les cas les plus complexes. Ainsi, trois ans après l’avoir exprimé, le thermodynamicien Robert Mayer en développa-t-il les conséquences pour les êtres vivants, notamment pour les végétaux, qui absorbent de la lumière et la convertissent partie en chaleur, partie en énergie chimique (énergie de liaison), au cours de la photosynthèse (1845). Le même raisonnement s’applique aux animaux, qui utilisent de l’énergie chimique et la convertissent partie en travail (mouvements), partie en chaleur.Le second principe, ou principe de l’augmentation de l’entropie , peut être énoncé de différentes façons, suivant le domaine auquel on l’applique.En bioénergétique, l’énoncé statistique est le plus commode.Un même état macroscopique observable correspond à un très grand nombre d’états microscopiques différents indiscernables, appelés complexions. On admet habituellement que toutes les complexions sont équiprobables et qu’un état macroscopique a d’autant plus de chances de se réaliser qu’il correspond à un plus grand nombre de complexions; ce nombre est appelé sa probabilité thermodynamique W. On appelle entropie la grandeur
La formation d’une molécule-gramme de glucose correspond à une accumulation d’énergie équivalente à 2 900 kJ, dans l’air, à la pression atmosphérique.Diverses bactéries, autotrophes également, tirent l’énergie qui leur est nécessaire de l’oxydation de substances minérales présentes dans le sol ou les eaux: sels ammoniacaux, nitrates, sulfures... Leur chimiosynthèse est beaucoup moins importante quantitativement que la photosynthèse, aussi la majeure partie de l’énergie externe captée par les êtres vivants provient-elle originellement de la lumière solaire.Les organismes hétérotrophes, animaux, bactéries, champignons, oxydant des substances organiques élaborées par les autotrophes, utilisent l’énergie de liaison chimique des substances synthétisées par les précédents. Les cellules non chlorophylliennes des végétaux autotrophes font de même.Une des caractéristiques des phénomènes bioénergétiques est qu’ils se réalisent à température sensiblement constante. Cela est exact pour nos propres cellules, bien que leur respiration s’accompagne d’une production de chaleur. Mais l’excédent en est immédiatement dissipé.Il en est à peu près de même pour un végétal. Si sa marge thermique interne n’est pas soumise à une régulation aussi poussée que celle de notre corps, cet organisme fonctionne cependant à température sensiblement uniforme dans une gamme comprise entre 0 et 40 0C.Les principes de la thermodynamique et la bioénergétiqueHistoriquement, les phénomènes énergétiques ont d’abord été étudiés à propos des machines à vapeur. Une science s’est ainsi édifiée, qui s’applique à tous les domaines de la physique, de la chimie et de la biologie. Son importance est fondamentale et son application universelle, bien qu’elle ait conservé le nom de thermodynamique.La thermodynamique repose sur deux principes qui ne sont pas directement démontrables avec précision. On considère, cependant, qu’ils sont amplement vérifiés par l’ensemble des conséquences qu’on en a tirées.Le premier principe , ou principe de la conservation de l’énergie , énonce que l’énergie ne peut être ni créée, ni détruite, et que, notamment, la chaleur et le travail en sont deux formes équivalentes. Un système physique (ou un être vivant) qui échange de l’énergie avec l’extérieur subit une variation de son énergie interne. La somme de chaleur perdue et de travail effectué par le système considéré est intégralement reçue par ce qui l’entoure. La validité de ce principe, en biologie, s’impose aisément à l’esprit, même dans les cas les plus complexes. Ainsi, trois ans après l’avoir exprimé, le thermodynamicien Robert Mayer en développa-t-il les conséquences pour les êtres vivants, notamment pour les végétaux, qui absorbent de la lumière et la convertissent partie en chaleur, partie en énergie chimique (énergie de liaison), au cours de la photosynthèse (1845). Le même raisonnement s’applique aux animaux, qui utilisent de l’énergie chimique et la convertissent partie en travail (mouvements), partie en chaleur.Le second principe, ou principe de l’augmentation de l’entropie , peut être énoncé de différentes façons, suivant le domaine auquel on l’applique.En bioénergétique, l’énoncé statistique est le plus commode.Un même état macroscopique observable correspond à un très grand nombre d’états microscopiques différents indiscernables, appelés complexions. On admet habituellement que toutes les complexions sont équiprobables et qu’un état macroscopique a d’autant plus de chances de se réaliser qu’il correspond à un plus grand nombre de complexions; ce nombre est appelé sa probabilité thermodynamique W. On appelle entropie la grandeur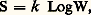 Le second principe, qui apparaît alors comme une conséquence des hypothèses faites ci-dessus, énonce que l’entropie d’un système isolé ne peut aller qu’en croissant.On admet traditionnellement qu’un système qui évolue va vers des états de plus en plus désordonnés. D’autre part, comme dans le seul cas analysable, celui des gaz parfaits, la répartition des constituants, de simples molécules en l’occurrence, tend à être quasi uniforme; il est généralement admis qu’il en va de même pour tout système. En conséquence, tout système tendrait vers un état de désordre aussi grand que possible caractérisé par une quasi-uniformité de la répartition de ses constituants.Cette manière de voir rend difficilement compréhensible l’apparition de structures très ordonnées dans les êtres vivants, puisque cette apparition d’ordre devrait correspondre à une diminution spontanée d’entropie. On explique cette anomalie en disant que cette diminution serait surcompensée par l’augmentation d’entropie des constituants des aliments transformés en excréta.D’après certains auteurs, l’apparition de structures serait explicable en recourant à un mode particulier d’exposition de la thermodynamique, la «thermodynamique des phénomènes irréversibles». On établit dans cette théorie que, lorsqu’un phénomène se déroule loin de l’équilibre, il peut apparaître des «structures dissipatives» consistant en phénomènes cycliques correspondant à une «dégradation» de l’énergie.Il n’en reste pas moins que l’apparition locale de structures est en contradiction avec une quasi-uniformisation de la répartition des constituants. La tendance aussi bien vers la quasi-uniformité que vers un désordre croissant a été contestée récemment. En effet, on constate bien qu’un ordre imposé à un système est le plus souvent bouleversé lors de son évolution spontanée, mais cela n’exclut pas que le système tende vers un ordre qui lui est propre. Or, tout système tend vers un état d’équilibre, et dans un état d’équilibre il se produit une compensation entre les forces s’exerçant dans le système. Une compensation entre forces exige une disposition particulière des constituants, donc un certain ordre. D’autre part, dans les systèmes autres que les gaz parfaits, il existe entre les constituants des interactions qui s’opposent à une uniformisation de leur répartition. Enfin, l’augmentation de l’entropie, c’est-à-dire du nombre de complexions de l’état d’équilibre, correspond à une augmentation du nombre des constituants indépendants et de leurs interactions, donc à une possibilité de diversification croissante des situations à l’intérieur du système. Un système qui évolue ne deviendrait donc pas plus désordonné mais plus compliqué.En tout état de cause, il faut remarquer qu’un être vivant hétérotrophe adulte en phase d’entretien reste identique à lui-même en moyenne; par conséquent, son entropie ne varie pas. Les réactions dont il est le siège peuvent se faire grâce à l’augmentation de l’entropie des constituants de ses aliments passés à l’état d’excréta, donc de l’entropie du milieu extérieur.Les hétérotrophes dans leur phase de croissance, et a fortiori les autotrophes, qui accumulent des éléments du milieu extérieur, constituent des systèmes ouverts pour lesquels la détermination d’une variation d’entropie n’a guère de sens. Néanmoins, toutes les réactions correspondantes s’accompagnent d’une augmentation globale d’entropie, compte tenu de l’énergie lumineuse absorbée dans la photosynthèse.La variation d’entropie de systèmes complexes qui évoluent spontanément n’est pas calculable. De plus, de tels systèmes, et notamment les êtres vivants, sont rarement isolés. Mais on démontre que, pour qu’une transformation à une température constante T, n’impliquant pas un apport de travail par le milieu extérieur, se produise spontanément dans un système non isolé, il faut que la variation d’une certaine grandeur, son énergie libre F, soit négative. La variation d’énergie libre est définie par la relation F= U 漣T S, où U est l’échange d’énergie proprement dite. Quand le milieu extérieur exerce une pression P, on doit remplacer F par l’enthalpie libre G définie par la relation G=F+PV, où V est le volume du système. Lorsque F ou G sont négatives, on dit que la transformation est exergonique. La transformation est endergonique dans le cas contraire.Les conversions d’énergieLes réactions biochimiques se déroulent à température sensiblement constante, les processus biologiques d’utilisation de l’énergie ne provoquant proportionnellement pas une augmentation d’entropie aussi importante que les machines thermiques qui fonctionnent en utilisant une différence de température suivant un principe complètement différent. Tandis que, dans un four solaire, la lumière absorbée par un corps noir est directement convertie en chaleur, les radiations visibles absorbées par la chlorophylle d’une plante se retrouvent sous la forme d’énergie chimique. Après consommation du végétal par un animal, cette énergie remaniée subsiste en partie dans les constituants nouveaux et elle est en partie dissipée en chaleur ou en travail, voire en électricité ou en lumière.Toutes les manifestations bioénergétiques dépendent de réactions chimiques. Une réaction endergonique ne peut se produire seule spontanément. Même la présence d’un catalyseur, d’une enzyme, n’y peut rien changer.Lorsqu’une réaction du type
Le second principe, qui apparaît alors comme une conséquence des hypothèses faites ci-dessus, énonce que l’entropie d’un système isolé ne peut aller qu’en croissant.On admet traditionnellement qu’un système qui évolue va vers des états de plus en plus désordonnés. D’autre part, comme dans le seul cas analysable, celui des gaz parfaits, la répartition des constituants, de simples molécules en l’occurrence, tend à être quasi uniforme; il est généralement admis qu’il en va de même pour tout système. En conséquence, tout système tendrait vers un état de désordre aussi grand que possible caractérisé par une quasi-uniformité de la répartition de ses constituants.Cette manière de voir rend difficilement compréhensible l’apparition de structures très ordonnées dans les êtres vivants, puisque cette apparition d’ordre devrait correspondre à une diminution spontanée d’entropie. On explique cette anomalie en disant que cette diminution serait surcompensée par l’augmentation d’entropie des constituants des aliments transformés en excréta.D’après certains auteurs, l’apparition de structures serait explicable en recourant à un mode particulier d’exposition de la thermodynamique, la «thermodynamique des phénomènes irréversibles». On établit dans cette théorie que, lorsqu’un phénomène se déroule loin de l’équilibre, il peut apparaître des «structures dissipatives» consistant en phénomènes cycliques correspondant à une «dégradation» de l’énergie.Il n’en reste pas moins que l’apparition locale de structures est en contradiction avec une quasi-uniformisation de la répartition des constituants. La tendance aussi bien vers la quasi-uniformité que vers un désordre croissant a été contestée récemment. En effet, on constate bien qu’un ordre imposé à un système est le plus souvent bouleversé lors de son évolution spontanée, mais cela n’exclut pas que le système tende vers un ordre qui lui est propre. Or, tout système tend vers un état d’équilibre, et dans un état d’équilibre il se produit une compensation entre les forces s’exerçant dans le système. Une compensation entre forces exige une disposition particulière des constituants, donc un certain ordre. D’autre part, dans les systèmes autres que les gaz parfaits, il existe entre les constituants des interactions qui s’opposent à une uniformisation de leur répartition. Enfin, l’augmentation de l’entropie, c’est-à-dire du nombre de complexions de l’état d’équilibre, correspond à une augmentation du nombre des constituants indépendants et de leurs interactions, donc à une possibilité de diversification croissante des situations à l’intérieur du système. Un système qui évolue ne deviendrait donc pas plus désordonné mais plus compliqué.En tout état de cause, il faut remarquer qu’un être vivant hétérotrophe adulte en phase d’entretien reste identique à lui-même en moyenne; par conséquent, son entropie ne varie pas. Les réactions dont il est le siège peuvent se faire grâce à l’augmentation de l’entropie des constituants de ses aliments passés à l’état d’excréta, donc de l’entropie du milieu extérieur.Les hétérotrophes dans leur phase de croissance, et a fortiori les autotrophes, qui accumulent des éléments du milieu extérieur, constituent des systèmes ouverts pour lesquels la détermination d’une variation d’entropie n’a guère de sens. Néanmoins, toutes les réactions correspondantes s’accompagnent d’une augmentation globale d’entropie, compte tenu de l’énergie lumineuse absorbée dans la photosynthèse.La variation d’entropie de systèmes complexes qui évoluent spontanément n’est pas calculable. De plus, de tels systèmes, et notamment les êtres vivants, sont rarement isolés. Mais on démontre que, pour qu’une transformation à une température constante T, n’impliquant pas un apport de travail par le milieu extérieur, se produise spontanément dans un système non isolé, il faut que la variation d’une certaine grandeur, son énergie libre F, soit négative. La variation d’énergie libre est définie par la relation F= U 漣T S, où U est l’échange d’énergie proprement dite. Quand le milieu extérieur exerce une pression P, on doit remplacer F par l’enthalpie libre G définie par la relation G=F+PV, où V est le volume du système. Lorsque F ou G sont négatives, on dit que la transformation est exergonique. La transformation est endergonique dans le cas contraire.Les conversions d’énergieLes réactions biochimiques se déroulent à température sensiblement constante, les processus biologiques d’utilisation de l’énergie ne provoquant proportionnellement pas une augmentation d’entropie aussi importante que les machines thermiques qui fonctionnent en utilisant une différence de température suivant un principe complètement différent. Tandis que, dans un four solaire, la lumière absorbée par un corps noir est directement convertie en chaleur, les radiations visibles absorbées par la chlorophylle d’une plante se retrouvent sous la forme d’énergie chimique. Après consommation du végétal par un animal, cette énergie remaniée subsiste en partie dans les constituants nouveaux et elle est en partie dissipée en chaleur ou en travail, voire en électricité ou en lumière.Toutes les manifestations bioénergétiques dépendent de réactions chimiques. Une réaction endergonique ne peut se produire seule spontanément. Même la présence d’un catalyseur, d’une enzyme, n’y peut rien changer.Lorsqu’une réaction du type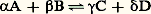 se déroule jusqu’à ce que les concentrations (A), (B), (C) et (D) de ses quatre participants aient atteint leur état final, la variation d’enthalpie libre est donnée par la relation:
se déroule jusqu’à ce que les concentrations (A), (B), (C) et (D) de ses quatre participants aient atteint leur état final, la variation d’enthalpie libre est donnée par la relation: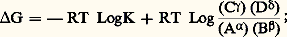 (R: constante des gaz parfaits; T: température absolue; Log K: logarithme népérien de la constante d’équilibre de la réaction).On peut, connaissant la valeur de K et les concentrations respectives initiales des quatre constituants mis en présence, prévoir si la réaction se déroulera de gauche à droite ou de droite à gauche. Si G est négatif, le premier sens sera spontané; ce sera le sens contraire si G est positif.Bien entendu, un appoint d’enthalpie libre, provenant du milieu extérieur dans des conditions convenables, permettra de réaliser une réaction endergonique. Cet appoint devra être plus élevé que le besoin.Les réactions coupléesGénéralement, l’élaboration du protoplasme par un organisme comprend une série complexe de réactions endergoniques, dont les besoins énergétiques sont couverts par une autre série complexe de réactions exergoniques. Globalement, les synthèses du protoplasme sont endergoniques, tandis que la respiration, processus de dégradation, est exergonique.L’ensemble des deux séries ne peut être énergétiquement dissocié. Dans le détail, l’énergie libérée par le processus exergonique ne peut être utilisée dans le processus endergonique qu’à la condition qu’un même groupe d’atomes, libéré dans une étape du premier, entre dans l’autre en «emportant» avec lui l’énergie nécessaire. Il doit exister nécessairement une relation quantitative d’atome à atome ou de molécule à molécule entre les deux réactions. On dit qu’elles sont couplées.On aura schématiquement:
(R: constante des gaz parfaits; T: température absolue; Log K: logarithme népérien de la constante d’équilibre de la réaction).On peut, connaissant la valeur de K et les concentrations respectives initiales des quatre constituants mis en présence, prévoir si la réaction se déroulera de gauche à droite ou de droite à gauche. Si G est négatif, le premier sens sera spontané; ce sera le sens contraire si G est positif.Bien entendu, un appoint d’enthalpie libre, provenant du milieu extérieur dans des conditions convenables, permettra de réaliser une réaction endergonique. Cet appoint devra être plus élevé que le besoin.Les réactions coupléesGénéralement, l’élaboration du protoplasme par un organisme comprend une série complexe de réactions endergoniques, dont les besoins énergétiques sont couverts par une autre série complexe de réactions exergoniques. Globalement, les synthèses du protoplasme sont endergoniques, tandis que la respiration, processus de dégradation, est exergonique.L’ensemble des deux séries ne peut être énergétiquement dissocié. Dans le détail, l’énergie libérée par le processus exergonique ne peut être utilisée dans le processus endergonique qu’à la condition qu’un même groupe d’atomes, libéré dans une étape du premier, entre dans l’autre en «emportant» avec lui l’énergie nécessaire. Il doit exister nécessairement une relation quantitative d’atome à atome ou de molécule à molécule entre les deux réactions. On dit qu’elles sont couplées.On aura schématiquement: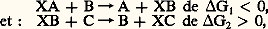 de sorte qu’on observe globalement:
de sorte qu’on observe globalement: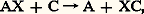 avec
avec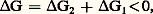 l’ensemble se soldant par une diminution d’enthalpie libre , un bilan exergonique.Le métabolisme intermédiaireNos aliments sont constitués de molécules relativement stables: glucides, protides, lipides... Prenons le cas des premiers. On peut les faire brûler, c’est-à-dire obtenir, par oxydation, de l’énergie calorifique. Notre organisme réalise aussi des oxydations qui peuvent aboutir aux mêmes résultats matériels: formation de gaz carbonique et d’eau. Lavoisier comparait avec raison la respiration à la combustion. Dans les deux modalités de dégradation, le bilan énergétique est le même.Mais la modalité biologique diffère de la combustion en ce que la chaleur libérée ne l’est que très progressivement, de sorte qu’elle peut se dissiper à l’extérieur sans que la température de notre corps s’élève et sans que nos protéines thermolabiles en souffrent. D’ailleurs, toutes les réactions ont lieu entre substances en solution dans l’eau, milieu à forte capacité calorifique, donc déjà thermiquement tamponné. D’autre part, l’oxygène n’intervient pas intempestivement, les étapes intermédiaires de l’oxydation des glucides sont multiples, chaque molécule est dégradée d’une manière très progressive, avec des «chutes» d’enthalpie libre petites qui se succèdent en cascades et non en cataractes. Cette progressivité, à la température de notre corps, est rendue possible par les enzymes qui catalysent une succession de réactions dont chacune n’est qu’une petite modification du métabolite provenant de la réaction précédente.Les réactions fondamentales sont des oxydoréductions de métabolites «électroactifs», c’est-à-dire des échanges d’électrons. Ils s’accompagnent le plus souvent d’échanges de protons et apparaissent alors comme des échanges d’hydrogène.La formulation la plus générale est:
l’ensemble se soldant par une diminution d’enthalpie libre , un bilan exergonique.Le métabolisme intermédiaireNos aliments sont constitués de molécules relativement stables: glucides, protides, lipides... Prenons le cas des premiers. On peut les faire brûler, c’est-à-dire obtenir, par oxydation, de l’énergie calorifique. Notre organisme réalise aussi des oxydations qui peuvent aboutir aux mêmes résultats matériels: formation de gaz carbonique et d’eau. Lavoisier comparait avec raison la respiration à la combustion. Dans les deux modalités de dégradation, le bilan énergétique est le même.Mais la modalité biologique diffère de la combustion en ce que la chaleur libérée ne l’est que très progressivement, de sorte qu’elle peut se dissiper à l’extérieur sans que la température de notre corps s’élève et sans que nos protéines thermolabiles en souffrent. D’ailleurs, toutes les réactions ont lieu entre substances en solution dans l’eau, milieu à forte capacité calorifique, donc déjà thermiquement tamponné. D’autre part, l’oxygène n’intervient pas intempestivement, les étapes intermédiaires de l’oxydation des glucides sont multiples, chaque molécule est dégradée d’une manière très progressive, avec des «chutes» d’enthalpie libre petites qui se succèdent en cascades et non en cataractes. Cette progressivité, à la température de notre corps, est rendue possible par les enzymes qui catalysent une succession de réactions dont chacune n’est qu’une petite modification du métabolite provenant de la réaction précédente.Les réactions fondamentales sont des oxydoréductions de métabolites «électroactifs», c’est-à-dire des échanges d’électrons. Ils s’accompagnent le plus souvent d’échanges de protons et apparaissent alors comme des échanges d’hydrogène.La formulation la plus générale est: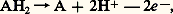 couplée avec
couplée avec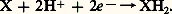 Parmi les intermédiaires de plus en plus oxydés, figurent des acides organiques. Ainsi, l’acide 6-phosphogluconique, dérivé du glucose 6-phosphate, est formé au cours de la réaction 1.Tandis que le glucose est oxydé, le NADP+, ou nicotinamide adénine dinucléotide phosphate, est réduit en NADPH+H+.Mais, dans de nombreux cas, l’accepteur d’électrons n’est pas accepteur de protons. Il en est ainsi pour les cytochromes, pigments rouges des cellules de tous les organismes aérobies. Ils renferment du fer qui passe de l’état oxydé ferrique Fe+++ à l’état ferreux Fe++ et vice versa par gain ou perte d’électron.La série des oxydoréductions terminales de la respiration comprend un transfert d’électrons finalement acceptés par l’oxygène. Ce dernier, chargé négativement, s’unit aux protons pour former de l’eau (réactions 2).Ces transferts d’électrons s’accompagnent de transferts d’énergie avec perte, chaque étape correspondant à une chute moyenne de potentiel E de 200 à 400 millivolts par électron-gramme.La capacité pour une substance de céder un électron à une autre peut être déterminée par la mesure du potentiel d’oxydoréduction de leur solution.En prenant comme référence l’électrode normale à hydrogène, il est possible de mesurer une différence de potentiel négative si les électrons vont de la solution à l’électrode à hydrogène et positive dans le cas inverse. Dans des conditions de pH, de concentration et de température déterminées, on dispose ainsi d’une mesure du pouvoir réducteur des différents transferts d’électrons. Les transferts se font toujours spontanément de telle sorte qu’ils correspondent à une diminution d’enthalpie libre. Celle-ci peut être exprimée en joules, puisque la variation de potentiel est:
Parmi les intermédiaires de plus en plus oxydés, figurent des acides organiques. Ainsi, l’acide 6-phosphogluconique, dérivé du glucose 6-phosphate, est formé au cours de la réaction 1.Tandis que le glucose est oxydé, le NADP+, ou nicotinamide adénine dinucléotide phosphate, est réduit en NADPH+H+.Mais, dans de nombreux cas, l’accepteur d’électrons n’est pas accepteur de protons. Il en est ainsi pour les cytochromes, pigments rouges des cellules de tous les organismes aérobies. Ils renferment du fer qui passe de l’état oxydé ferrique Fe+++ à l’état ferreux Fe++ et vice versa par gain ou perte d’électron.La série des oxydoréductions terminales de la respiration comprend un transfert d’électrons finalement acceptés par l’oxygène. Ce dernier, chargé négativement, s’unit aux protons pour former de l’eau (réactions 2).Ces transferts d’électrons s’accompagnent de transferts d’énergie avec perte, chaque étape correspondant à une chute moyenne de potentiel E de 200 à 400 millivolts par électron-gramme.La capacité pour une substance de céder un électron à une autre peut être déterminée par la mesure du potentiel d’oxydoréduction de leur solution.En prenant comme référence l’électrode normale à hydrogène, il est possible de mesurer une différence de potentiel négative si les électrons vont de la solution à l’électrode à hydrogène et positive dans le cas inverse. Dans des conditions de pH, de concentration et de température déterminées, on dispose ainsi d’une mesure du pouvoir réducteur des différents transferts d’électrons. Les transferts se font toujours spontanément de telle sorte qu’ils correspondent à une diminution d’enthalpie libre. Celle-ci peut être exprimée en joules, puisque la variation de potentiel est: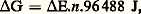 E étant exprimé en volts, 96 488 coulombs (Faraday) étant la quantité d’électricité qui correspond au départ d’un électron-gramme et n le nombre d’électrons labiles concernés.Les liaisons «riches en énergie»Les oxydations successives des métabolites libèrent au total une quantité d’énergie importante qui est utilisée pour un grand nombre de synthèses. Pour beaucoup de ces synthèses et pour les besoins énergétiques courants de l’organisme, l’énergie est fournie en quantité convenable par la rupture de liaisons esterphosphoriques, dans des pyrophosphates organiques généralement. Celui qui intervient le plus souvent est l’adénosine triphosphate, ou ATP. L’hydrolyse d’une liaison pyrophosphate de ce corps, avec libération de l’acide adénosine diphosphorique et de phosphate minéral, selon la réaction
E étant exprimé en volts, 96 488 coulombs (Faraday) étant la quantité d’électricité qui correspond au départ d’un électron-gramme et n le nombre d’électrons labiles concernés.Les liaisons «riches en énergie»Les oxydations successives des métabolites libèrent au total une quantité d’énergie importante qui est utilisée pour un grand nombre de synthèses. Pour beaucoup de ces synthèses et pour les besoins énergétiques courants de l’organisme, l’énergie est fournie en quantité convenable par la rupture de liaisons esterphosphoriques, dans des pyrophosphates organiques généralement. Celui qui intervient le plus souvent est l’adénosine triphosphate, ou ATP. L’hydrolyse d’une liaison pyrophosphate de ce corps, avec libération de l’acide adénosine diphosphorique et de phosphate minéral, selon la réaction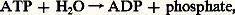 libère l’équivalent de 33 kJ par molécule-gramme. On attribue le caractère exergonique de cette rupture au fait que le phosphate formé possède une énergie de résonance plus élevée que le composé phosphorylé initial. Son énergie de formation étant plus faible que celle du pyrophosphate organique, la différence se trouve libérée. Ce dégagement tient aux propriétés de l’ensemble de chacune des deux molécules intéressées par cette réaction (ATP et H2O). Bien qu’il soit inexact d’attribuer l’énergie ainsi libérée à la liaison elle-même, le qualificatif de liaison «riche» reste universellement adopté. On le désigne par le signe 黎.D’autres nucléotides pyrophosphates, d’autres composés phosphorylés sont «riches» d’énergie labile. Dans tous les cas, la liaison rompue par hydrolyse est celle qui unit un ion acide comme l’ion orthophosphate à un autre acide engagé dans une molécule organique (celle-ci est soit phosphorylée, soit acide, parce qu’elle possède un groupement carboxyle (acétyl 黎 phosphate). Une liaison «riche» peut aussi exister entre un acide sulfhydrylé et un acide organique.La formation des liaisons «riches» exige toujours plus d’énergie que n’en libère leur rupture. Elle est jumelée aux transferts d’électrons et de protons qui interviennent soit entre transporteurs excités par voie photochimique dans les chloroplastes des végétaux chlorophylliens (il s’agit alors de photophosphorylation), soit entre transporteurs intermédiaires des oxydations respiratoires dont le siège se situe dans les mitochondries (il s’agit alors d’oxydations phosphorylantes). L’oxydation complète d’une molécule-gramme de glucose peut donner 38 liaisons pyrophosphates de l’ATP, soit l’équivalent de 1 250 kJ, avec un rendement de 40 p. 100.L’ATP est toujours présent dans les cellules vivantes. Il fournit de l’énergie à la plupart des synthèses, aux mouvements de nos muscles, à l’émission de lumière des organismes luminescents. Il représente la forme énergétique la plus commode et mérite le nom de «petite monnaie» de l’énergie selon une expression du biochimiste Szent-Gyorgýi.Le rendement énergétiqueIl n’est pas raisonnable de comparer le rendement énergétique d’un être vivant à celui d’une machine à vapeur. La comparaison n’a pas de sens. Le rendement d’un être vivant est le quotient:
libère l’équivalent de 33 kJ par molécule-gramme. On attribue le caractère exergonique de cette rupture au fait que le phosphate formé possède une énergie de résonance plus élevée que le composé phosphorylé initial. Son énergie de formation étant plus faible que celle du pyrophosphate organique, la différence se trouve libérée. Ce dégagement tient aux propriétés de l’ensemble de chacune des deux molécules intéressées par cette réaction (ATP et H2O). Bien qu’il soit inexact d’attribuer l’énergie ainsi libérée à la liaison elle-même, le qualificatif de liaison «riche» reste universellement adopté. On le désigne par le signe 黎.D’autres nucléotides pyrophosphates, d’autres composés phosphorylés sont «riches» d’énergie labile. Dans tous les cas, la liaison rompue par hydrolyse est celle qui unit un ion acide comme l’ion orthophosphate à un autre acide engagé dans une molécule organique (celle-ci est soit phosphorylée, soit acide, parce qu’elle possède un groupement carboxyle (acétyl 黎 phosphate). Une liaison «riche» peut aussi exister entre un acide sulfhydrylé et un acide organique.La formation des liaisons «riches» exige toujours plus d’énergie que n’en libère leur rupture. Elle est jumelée aux transferts d’électrons et de protons qui interviennent soit entre transporteurs excités par voie photochimique dans les chloroplastes des végétaux chlorophylliens (il s’agit alors de photophosphorylation), soit entre transporteurs intermédiaires des oxydations respiratoires dont le siège se situe dans les mitochondries (il s’agit alors d’oxydations phosphorylantes). L’oxydation complète d’une molécule-gramme de glucose peut donner 38 liaisons pyrophosphates de l’ATP, soit l’équivalent de 1 250 kJ, avec un rendement de 40 p. 100.L’ATP est toujours présent dans les cellules vivantes. Il fournit de l’énergie à la plupart des synthèses, aux mouvements de nos muscles, à l’émission de lumière des organismes luminescents. Il représente la forme énergétique la plus commode et mérite le nom de «petite monnaie» de l’énergie selon une expression du biochimiste Szent-Gyorgýi.Le rendement énergétiqueIl n’est pas raisonnable de comparer le rendement énergétique d’un être vivant à celui d’une machine à vapeur. La comparaison n’a pas de sens. Le rendement d’un être vivant est le quotient: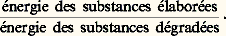 Le travail éventuellement extériorisé, de même que le travail lié à l’absorption, à la circulation des aliments, aux mouvements intracellulaires ou au travail interne des organes, est produit par la consommation d’une fraction des aliments ou d’une fraction des substances élaborées.Le rendement d’une machine thermique n’est que le quotient:
Le travail éventuellement extériorisé, de même que le travail lié à l’absorption, à la circulation des aliments, aux mouvements intracellulaires ou au travail interne des organes, est produit par la consommation d’une fraction des aliments ou d’une fraction des substances élaborées.Le rendement d’une machine thermique n’est que le quotient: Dans les cas les plus simples, quelques bilans de transformations de matière expriment la satisfaction des divers besoins cellulaires.Ainsi, pour une jeune culture de moisissure (Aspergillus ), le rendement matériel de croissancemasse de protoplasme formé/masse d’aliment consomméest de l’ordre de 40 p. 100. Pour une colonie bactérienne en cours de multiplication, il n’est que de 20 p. 100. Autrement dit, 60 ou 80 p. 100 des aliments absorbés sont dégradés, alors que 40 ou 20 p. 100 de leurs chaînes carbonées sont transformés en constituants protoplasmiques.La quasi-totalité de l’énergie libérée par la dégradation, c’est-à-dire par la respiration, est dissipée sous forme de chaleur. Une très faible fraction de cette énergie (quelques pourcent au plus) se retrouve dans l’énergie chimique des constituants du protoplasme. Ces constituants ont avant tout conservé l’énergie chimique présente dans les molécules des aliments.Le rendement est certainement plus faible encore pour un organisme homéotherme qui utilise une partie importante de ses aliments au maintien de son équilibre thermique.Pour un végétal chlorophyllien, à la lumière, le rendement énergétique de la photosynthèse peut atteindre 30 p. 100 dans les meilleures conditions d’utilisation de l’énergie lumineuse. Mais, dans la nature, il ne dépasse pas 1 ou 2 p. 100 de l’énergie lumineuse qui arrive au sol.
Dans les cas les plus simples, quelques bilans de transformations de matière expriment la satisfaction des divers besoins cellulaires.Ainsi, pour une jeune culture de moisissure (Aspergillus ), le rendement matériel de croissancemasse de protoplasme formé/masse d’aliment consomméest de l’ordre de 40 p. 100. Pour une colonie bactérienne en cours de multiplication, il n’est que de 20 p. 100. Autrement dit, 60 ou 80 p. 100 des aliments absorbés sont dégradés, alors que 40 ou 20 p. 100 de leurs chaînes carbonées sont transformés en constituants protoplasmiques.La quasi-totalité de l’énergie libérée par la dégradation, c’est-à-dire par la respiration, est dissipée sous forme de chaleur. Une très faible fraction de cette énergie (quelques pourcent au plus) se retrouve dans l’énergie chimique des constituants du protoplasme. Ces constituants ont avant tout conservé l’énergie chimique présente dans les molécules des aliments.Le rendement est certainement plus faible encore pour un organisme homéotherme qui utilise une partie importante de ses aliments au maintien de son équilibre thermique.Pour un végétal chlorophyllien, à la lumière, le rendement énergétique de la photosynthèse peut atteindre 30 p. 100 dans les meilleures conditions d’utilisation de l’énergie lumineuse. Mais, dans la nature, il ne dépasse pas 1 ou 2 p. 100 de l’énergie lumineuse qui arrive au sol.
bioénergétique [ bjoenɛrʒetik ] adj.• 1911; de bio- et énergétique♦ Didact. Qui concerne les transformations de l'énergie dans les tissus vivants. — N. f. La bioénergétique.
● bioénergétique adjectif Relatif à la bioénergie.bioénergétiqueadj. et n. f. BIOLd1./d adj. Dont les êtres vivants tirent de l'énergie. Les sucres sont bioénergétiques.d2./d n. f. Partie de la biochimie qui étudie les transformations que les êtres vivants font subir aux différentes formes d'énergie (lumière, chaleur, etc.).bioénergétique [bjoenɛʀʒetik] n. f.ÉTYM. 1911; de bio-, et énergétique.❖♦ Didact. Partie de la physiologie qui traite des transformations de l'énergie dans les tissus vivants. || « Chaleur animale et bioénergétique » (J. Lefèvre).
Encyclopédie Universelle. 2012.
